〖がん検診AI〗 AI読影は医師を置き換えるのか──規制改革会議資料から読む「見逃しを減らす医療AI」の実装論
グロッサリー(用語集)
対策型検診: 市町村などが公共政策として実施するがん検診です。個人の任意検査ではなく、集団全体の利益と不利益のバランスが問われます。
二重読影: 画像検査などで、複数の読影者が確認することで見落としを減らす仕組みです。
AI読影補助: 画像上の異常候補を示す、優先順位を付ける、見落としやすい領域を再確認させるなど、医師の判断を支援するAIです。
SaMD: Software as a Medical Deviceの略です。日本語では、医療機器として扱われ得るプログラムを指します。
Human-in-the-Loop: AIが出した結果を、人間が確認・修正・最終判断する運用設計です。
要精検率: がん検診で、精密検査が必要と判定された人の割合です。AI導入後の過剰な陽性判定を監視する指標になります。
偽陽性割合: がんではないのに陽性または要精検と判定される割合です。検診では見逃しを減らすだけでなく、不必要な不安や検査も抑える必要があります。
免責事項・利益相反開示
本稿は、公開されている政府資料、厚生労働省資料、PMDA資料に基づく一般的な解説です。
個別施設の医療機器該当性判断、自治体の検診運用、法的責任判断を代替するものではありません。
筆者は医療AI、医療DX、AIガバナンスに関する研究、教育、事業開発に関与しています。本稿は公開情報の整理と実務上の論点提示を目的としており、特定製品の導入を推奨するものではありません。
はじめに — 問うべきは「置き換え」ではありません
医療AIの議論では、何度も同じ問いが立ち上がります。
「AIは医師を置き換えるのでしょうか」
がん検診AI、とくに読影補助AIについても、この問いは避けられません。
画像上の異常候補をAIが示せるなら、二重読影の一部をAIに置き換えられるのではないか。
読影医が足りない地域では、そのほうが現実的ではないか。
この期待は、現場感覚としてよく理解できます。
ただし、医療AIを制度の中に入れるとき、問いの立て方は変える必要があります。
本当に問うべきなのは、AIが医師を置き換えるかどうかではありません。
検診制度の精度管理の中で、AIをどこに置けば見逃しを減らせるのか。
この問いです。
がん検診AIは、置き換えの物語ではありません。
見逃しを減らし、不必要な精密検査を増やしすぎず、医師が説明できる形で運用するための「精度保証」の物語として読むべきです。
要点: がん検診AIの本質は、医師代替ではなく精度管理です。AIが異常候補を示せることと、検診制度の中で安全に使えることは同じではありません。
第1章: 一次情報で見る「現時点の線引き」
規制改革推進会議の健康・医療・介護ワーキンググループでは、がん検診におけるAI読影補助が議論されています[1]。
https://www8.cao.go.jp/kisei-kaikaku/kisei/meeting/wg/2501_02medical/260212/medical09_0103.pdf
ここで重要なのは、AI活用の方向性が示されている一方で、制度側がかなり慎重に線を引いている点です。
同資料では、現時点では「一人の読影者による読影にAI読影補助を併用した場合に、二重読影と比較して、がん検診で同等以上の精度を有するとのエビデンスはない」と整理されています[1]。
これは、AIを否定しているという意味ではありません。
むしろ、読影機器やAI技術の進歩を踏まえ、効率的に読影する手法の是非を検討する余地は見ています。
ただし、対策型検診は「感度が高そうだから入れる」で済む領域ではありません。
偽陽性、偽陰性、追加検査の負担、過剰診断、地域間格差、精度管理まで含めて設計する必要があります。
数字で見ると、この慎重さには理由があります。
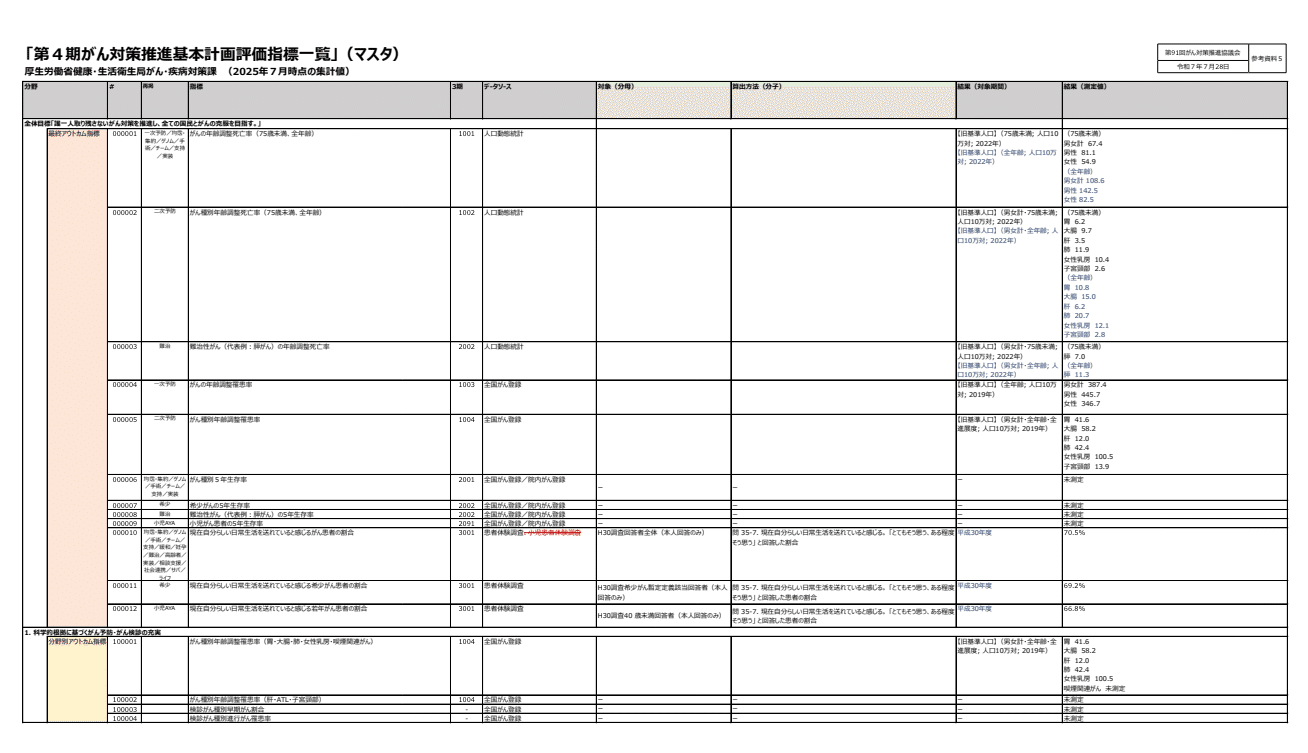
厚生労働省の第4期がん対策推進基本計画評価指標一覧では、令和4年度のがん検診受診率が整理されています[3]。
https://www.mhlw.go.jp/content/10901000/001526712.pdf
具体的には、胃がん48.4%、大腸がん45.9%、肺がん49.7%、乳がん47.4%、子宮頸がん43.6%です[3]。
これは国民生活基礎調査2022をもとにした指標値です。
がん種ごとに対象年齢や受診間隔の定義が違う点には注意が必要ですが、がん検診受診率60%達成に向けた集中キャンペーンの文脈が続く一方で、現実の受診率はまだ5割前後にとどまっています[3]。
さらに、令和2年度の精密検査受診率を見ると、胃X線79.7%、胃内視鏡92.6%、大腸70.2%、肺82.6%、乳89.8%、子宮頸76.6%です[3]。
がん発見率は、胃X線0.071%、胃内視鏡0.200%、大腸0.157%、肺0.027%、乳0.308%、子宮頸0.026%とされています[3]。
偽陽性割合は、胃X線5.9%、胃内視鏡6.6%、大腸6.1%、肺1.5%、乳6.3%、子宮頸2.5%です[3]。
つまり、AIの導入は単に「見つける力」を上げる話ではありません。
要精検率、精検受診率、がん発見率、偽陽性割合を同時に見なければ、受診者にとっての利益と不利益を評価できません。
指針上の対象者と間隔も、AI導入の前提になります。
厚労省指針では、胃がん検診は50歳以上で2年に1回、肺がん・乳がん・大腸がん検診は40歳以上です[2][4]。
肺と大腸は年1回、乳は2年に1回と整理されています[2][4]。
子宮頸がん検診は、細胞診は20歳以上を対象に原則2年に1回です。HPV検査単独法は30歳以上を対象に原則5年に1回とされ、追跡検査や実施体制の要件も伴います[4]。
https://www.mhlw.go.jp/content/10900000/001642974.pdf
肺がん検診の胸部エックス線読影は、「2名以上の医師」が読影し、そのうち1名は十分な経験を有する者とされています[2]。
ここに、医療AIの難しさがあります。
AIが異常候補を拾えることと、検診制度の中で安全に使えることは同じではありません。
前者は技術性能の話です。
後者は、運用と責任分界の話です。
要点: がん検診AIは、感度だけで評価できません。要精検率、精検受診率、がん発見率、偽陽性割合まで含めて、制度としての利益と不利益を見ます。
第2章: 二重読影は「人を二人置くこと」だけではありません
二重読影は、単なる人員配置ではありません。
目的は、見逃しを減らし、判定の質を担保することです。
したがってAIを考えるなら、「AIが二人目の医師になるか」ではなく、次の問いに分解したほうが現実的です。
AIはどの種類の病変を拾いやすいのでしょうか。
AIはどの種類の病変を拾いにくいのでしょうか。
AIの結果を医師が見る順番は、見逃しを減らすのでしょうか。それともアンカリングを増やすのでしょうか。
AIが陽性候補を示した場合、医師はどの手順で再確認するのでしょうか。
AIが何も示さなかった場合、医師は通常読影をどこまで維持するのでしょうか。
バージョン更新後に性能が変わったとき、施設はどう検証するのでしょうか。
この分解をせずに「AIで二重読影を代替できる」と言ってしまうと、実装は危うくなります。
規制改革推進会議の提出資料では、AIの期待される有用性として、見落とし防止、読影負荷の軽減、定型所見の検出支援が挙げられています[1]。
一方で、限界として、学習データ依存、稀少病変・非典型像の検出に限界、がん鑑別の不確実性も示されています[1]。
運用原則としては、AI使用時の記録・明示、最終診断・判定は医師が実施すること、管理指針・ガイドラインに沿った利用が挙げられています[1]。
性能値も慎重に読む必要があります。
同資料は、胸部単純X線写真や胸部CTを用いた肺結節検出AIの研究例を示しています[1]。
数値としては、AUC 0.982、感度79.0〜91.1%(Xp)・61.6〜98.1%(CT)、特異度93〜100%です[1]。
偽陽性数は、Xpで0.02〜0.34/例、CTで0.125〜32とされています[1]。
これは高性能を示す材料です。
しかし、研究条件、モダリティ、対象病変に依存する数値であり、対策型検診の全国実装成績そのものではありません。
低線量CT検診の根拠も、対象集団を切り分けて読む必要があります。
資料では、NLSTが53,454人、55〜74歳、喫煙指数600以上、肺癌死の相対危険度0.80と整理されています[1]。
NELSONは15,789人、50〜74歳、男性0.76、女性0.67と整理されています[1]。
重喫煙者集団では死亡率低減の可能性があります。
一方で、偽陽性や過剰診断も増えるという注意が併記されています[1]。
ここから言えるのは、「AIなら検診対象を広げてよい」ではありません。
対象者、検査法、害の評価を分けて設計する必要があるということです。
AIは疲れません。
大量の画像を一定の基準で見ることができます。
人間が見落としやすい微細な所見を候補として示せる可能性もあります。
これは大きな利点です。
一方で、AIは文脈を誤ります。
学習データと違う撮影条件、施設差、画像品質、稀な病変、非典型像、ラベルの偏りに弱い可能性があります。
PMDAのAI医療機器に関する専門部会でも、使用環境や入力データの違い、市販後の性能変化を含めた評価・管理が論点化されています[6][7]。
現場の医師がAIの苦手な領域を知らないまま使うと、「AIが何も言っていないから大丈夫」という逆方向の過信が起きます。
見逃しを減らすためのAIが、過信によって見逃しを増やす。
これは十分に起こり得ます。
要点: AIを「二人目の医師」として扱うと誤解が生まれます。AIは二重読影の思想を拡張する補助線にはなり得ますが、読影順序、再確認、陰性時の扱いまで設計して初めて安全に近づきます。
第3章: AI読影は精度より先に「手順」を決めます
がん検診AIの導入で最初に決めるべきなのは、モデル名ではありません。
手順です。
最低限、次のような設計が必要になります。
入力条件の固定。 どの撮影条件、どの画像形式、どの検査種別をAIに流すのかを決めます。
読影順序の設計。 医師が先に読むのか、AIの候補を先に見るのか、二段階で確認するのかを決めます。
再確認ルール。 AIが候補を示した場合に、どの所見を必ず再確認するかを定めます。
陰性時の扱い。 AIが候補を示さない場合でも、通常読影を省略しない条件を明確にします。
監査ログ。 AIのバージョン、入力画像、出力結果、最終判定、医師の修正理由を記録します。
性能劣化の監視。 施設ごとの偽陽性・偽陰性、要精検率、発見率、再読影結果を定期的に振り返ります。
このとき施設は、「AIが動いたか」ではなく、プロセス指標を先に置くべきです。
規制改革推進会議の提出資料は、肺がん検診文脈での提案例として、要精検率を初回8%、逐年5%を目安とし、AI導入後も継続的にモニタリングする必要性を示しています[1]。
もちろん、この数値を全てのがん種や全施設に横展開してよいわけではありません。
重要なのは、AI導入後も、要精検率や精検受診率を「見なくてよい指標」にしてはいけないという点です。
この設計がないAI導入は、単なる便利ツール導入で終わります。
医療AIで本当に難しいのは、アルゴリズムではありません。
臨床業務に組み込んだ後の品質管理です。
要点: AI読影の導入前に決めるべきものは、製品名ではなく手順です。入力条件、読影順序、陰性時の扱い、監査ログ、性能劣化監視がない導入は、検診制度の精度管理とは言えません。
第4章: 医師の責任はAI時代に軽くなりません
がん検診AIをめぐる議論で、もう一つ避けてはいけないのが責任分界です。
AIが候補を示します。
医師が最終判定します。
製造販売業者は、性能と安全性を説明します。
施設は、適切な利用条件を守ります。
行政は、制度として精度管理を設計します。
この役割分担を曖昧にしたまま導入すると、事故が起きたときに誰も説明できなくなります。
PMDA資料から見ても、AI医療機器はすでに抽象論の段階を出ています。
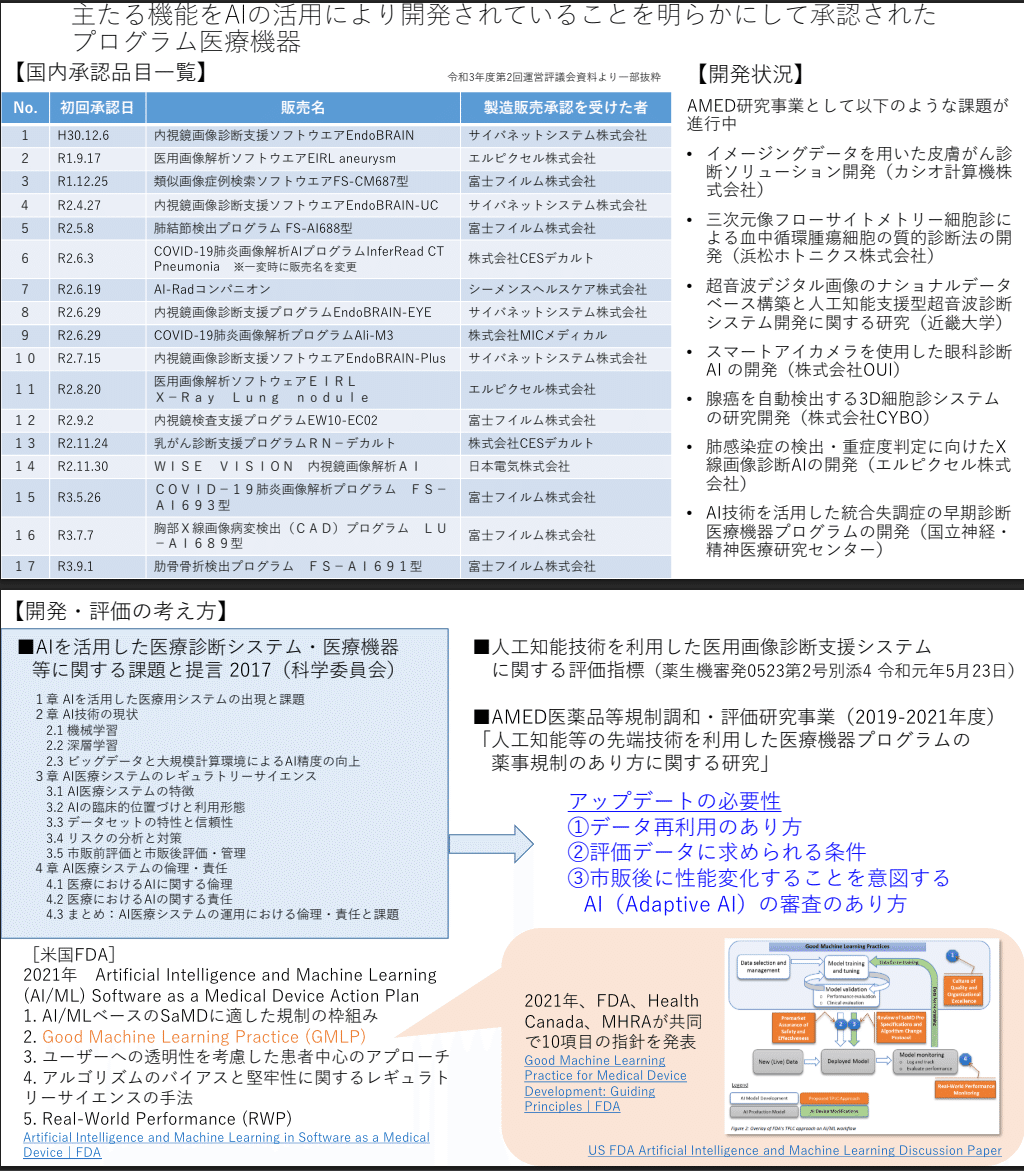
PMDAの資料「AI医療機器の開発状況等について」は、AIを活用して開発された承認済みプログラム医療機器を列挙しています[8]。
https://www.pmda.go.jp/files/000244149.pdf
対象は、平成30年12月6日のEndoBRAINから令和3年9月1日の肋骨骨折検出プログラムまでの17件です[8]。
ただし、この17件は令和3年度第2回運営評議会資料の一部抜粋です。
承認品目数そのものは時点依存であり、最新版の網羅的件数として扱うべきではありません。
さらにPMDAは、機械学習によって市販後性能が変化する性質を有するSaMDについて、開発・社会実装上の課題を整理しています[7]。
https://www.pmda.go.jp/files/000272867.pdf
検診AIを導入するなら、購入時の性能表だけでなく、バージョン更新、市販後の性能変化、施設ごとのデータ差、再評価の手順まで持たなければなりません。
ここで重要なのは、「最終判断は医師」と言えば済むわけではないことです。
最終判断が医師にあるなら、医師が判断できるだけの情報が必要です。
AIの適用条件、限界、バージョン、出力の意味、使ってはいけない場面が見える形で提供されなければなりません。
医師に責任を置くなら、医師に説明可能性を渡す必要があります。
この点で、がん検診AIは単なる医療機器導入ではありません。
現場の判断構造を設計し直すプロジェクトです。
要点: AI時代でも医師の責任は軽くなりません。むしろ、医師が最終判断を担うなら、適用条件、限界、バージョン、出力の意味を説明できる運用が必要になります。
第5章: がん検診AIを導入する前の実装チェックリスト
がん検診AIを検討する施設、自治体、開発者は、少なくとも次を確認する必要があります。
そのAIは医療機器プログラムに該当するのでしょうか。
承認、認証、届出など、制度上の位置づけは明示されているのでしょうか。
対象検査、対象年齢、対象画像、除外条件は明示されているのでしょうか。
AIの苦手な所見や適用外条件は、医師向けに説明されているのでしょうか。
読影順序と再確認手順は院内手順書に落ちているのでしょうか。
AI出力を見たことによるアンカリングを評価する設計はあるのでしょうか。
導入前後で、要精検率、精検受診率、がん発見率、偽陽性割合を比較するのでしょうか。
バージョン更新時に、再評価や研修を行うのでしょうか。
医師、技師、事務、自治体担当者の役割分担は明文化されているのでしょうか。
受診者に対して、AI利用の有無や説明方針をどう扱うかを決めているのでしょうか。
このチェックリストは、AI導入を止めるためのものではありません。
安全に前へ進めるためのものです。
医療AIを現場に入れるとき、最も危ないのは「性能が高いから大丈夫」という空気です。
性能が高いAIほど、運用が弱いと過信を生みます。
だからこそ、AI導入はモデル選定ではなく、運用設計から始めるべきです。
第6章: 最初の90日で何を決めるべきでしょうか
がん検診AIを検討する組織は、いきなり全面導入を目指さないほうが安全です。
最初の90日は、製品比較よりも「使う前提」を固める期間にすべきです。
第1に、対象範囲を決めます。
どのがん種、どの検査、どの画像、どの施設、どの読影体制で使うのかを明文化します。
ここが曖昧なままAIを入れると、製品の適用範囲と現場の使い方がずれます。
第2に、評価指標を決めます。
要精検率、精検受診率、がん発見率、偽陽性割合、再読影結果、医師の修正理由を、導入前から同じ定義で残します[3][4]。
導入後だけ数字を見ても、AIによって何が変わったのかは分かりません。
第3に、説明責任の流れを決めます。
医師、放射線技師、自治体担当者、医療機器メーカー、システム担当者の誰が、どの情報を確認し、どこまで記録するのかを整理します[5][9]。
第4に、更新時の再評価を決めます。
AI医療機器は、固定された機械ではありません。
モデル、学習データ、周辺システム、入力画像の条件が変われば、同じ施設でも性能や運用リスクが変わり得ます[7][10]。
この90日設計を省略すると、AI導入は「読影が速くなるか」という狭い議論に閉じます。
しかし、検診AIで本当に守るべきなのは速度だけではありません。
受診者の不利益を増やさず、見逃しを減らし、説明できる運用を維持することです。
要点: がん検診AIは、導入前90日の設計で成否が大きく変わります。対象範囲、評価指標、責任分界、更新時再評価を先に決めることで、AIを精度管理の中に置けます。
FAQ
Q1. AI読影補助は、二重読影の代わりになりますか。
現時点では、一般化して「代わりになる」とは言えません。
規制改革推進会議の提出資料では、一人読影にAI読影補助を併用した場合に、二重読影と同等以上の精度を有するとのエビデンスはないと整理されています[1]。
ただし、これはAI活用を否定するものではありません。
見落とし防止、読影負荷軽減、再確認支援として、どこに置くかを設計する段階だと読むべきです。
Q2. AIの感度が高ければ、検診に入れてよいのでしょうか。
感度だけでは不十分です。
検診では、偽陽性、要精検率、精検受診率、がん発見率、過剰診断、受診者の不安、医療資源への影響まで見ます。
AIが多く拾うほど良い、とは限りません。
Q3. 最終判断を医師にすれば、責任分界は十分でしょうか。
十分ではありません。
医師が最終判断するなら、医師がAIの適用条件、限界、バージョン、出力の意味を理解できる必要があります。
最終責任だけを医師に置き、説明可能性を渡さない運用は危険です。
Q4. 自治体や小規模施設は、何から始めるべきでしょうか。
まずは対象検査、対象画像、読影順序、再確認手順、ログ、評価指標を整理することです。
製品比較より先に、検診フローのどこでAIを使うのかを決める必要があります。
Q5. AI読影補助の導入で最も見落とされやすい論点は何でしょうか。
陰性時の扱いです。
AIが何も示さなかった場合に、通常読影をどこまで維持するのかを決めておかなければ、「AIが黙っているから大丈夫」という過信が起こり得ます。
おわりに — 置き換えではなく、精度保証の新しい二重化です
がん検診AIを「医師を置き換える技術」として語ると、議論は粗くなります。
本質は、AIが読影医の代わりになるかではありません。
検診という公共的な制度の中で、見逃しを減らし、不必要な不安や追加検査を増やしすぎず、医師が説明できる形でAIを組み込めるかです。
AIは二人目の医師ではありません。
しかし、よく設計されれば、二重読影の思想を拡張する補助線にはなり得ます。
置き換えではなく、精度保証の新しい二重化。
がん検診AIは、その言葉で議論したほうが現場に近いと考えます。
最後に、導入判断は一度で終わりません。
検診事業は年度ごとに対象者、委託先、読影体制、使用機器が変わることがあります。
そのたびに、AIの適用範囲、説明資料、精度指標、更新時の確認手順を見直す必要があります。
だからこそ、AI導入は単発の購入ではなく、検診制度の中に組み込む継続的な品質管理として扱うべきです。
本記事で綴った「AIに臨床の魂を宿す」という想いは、単なる思想の提唱に留まらず、具体的な「臨床現場への実装」へとフェーズを移行しました。
記事を読むだけでなく、実際に手を動かし、安全なガバナンスの下で臨床知を形式知・資産へと変えていくための実践的環境(Cursorvers Library)を公開しています。
その理念に共鳴し、評論家ではなく「実践者」として医療の未来の構築を志向される方は、是非メンバーシップ(無料・有料)への加入をご検討ください。
(もし不具合があれば、お問い合わせフォームからご連絡ください。)
▼ Cursorvers Program Roadmap
https://cursorvers.github.io/cursorvers-edu/services.html#phase01
参考文献
規制改革推進会議 健康・医療・介護WG 資料「がん検診におけるAI読影補助」。https://www8.cao.go.jp/kisei-kaikaku/kisei/meeting/wg/2501_02medical/260212/medical09_0103.pdf (確認日: 2026-04-14)
規制改革推進会議 健康・医療・介護WG 資料。https://www8.cao.go.jp/kisei-kaikaku/kisei/meeting/wg/2501_02medical/260212/medical09_0107.pdf (確認日: 2026-04-14)
厚生労働省「第4期がん対策推進基本計画評価指標一覧」。https://www.mhlw.go.jp/content/10901000/001526712.pdf (確認日: 2026-04-14)
厚生労働省「がん予防重点健康教育及びがん検診実施のための指針」。https://www.mhlw.go.jp/content/10900000/001642974.pdf (確認日: 2026-04-14)
厚生労働省「がん検診」。https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000059490.html (確認日: 2026-04-14)
PMDA「AIを活用したプログラム医療機器に関する専門部会」。https://www.pmda.go.jp/rs-std-jp/subcommittees/0024.html (確認日: 2026-04-14)
PMDA「レギュラトリーサイエンス活動報告書(2023年度)」。https://www.pmda.go.jp/files/000272867.pdf (確認日: 2026-04-14)
PMDA「AI医療機器の開発状況等について」。https://www.pmda.go.jp/files/000244149.pdf (確認日: 2026-04-14)
厚生労働省「医療機器プログラムについて」。https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000179749_00004.html (確認日: 2026-04-14)
PMDA「プログラム医療機器の承認審査に関する考え方」。https://www.pmda.go.jp/files/000273987.pdf (確認日: 2026-04-15)
#医療AI #がん検診 #AI読影 #画像診断 #SaMD #医療DX #PMDA #厚生労働省 #規制改革 #がん対策 #医師の働き方